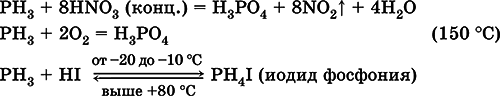Концентрированная кислота пассивирует Al, Be, Bi, Со, Cr, Fe, Ni и Pb, не реагирует с Au и Pt. Смесь HNO 3(конц.) и НCl (конц.) – « царская водка» – обладает еще более сильным окислительным действием: переводит в раствор золото и платину. Нитрующим началом HNO 3в ее реакциях с органическими веществами является ион NO 2 +( нитроил).
В отличие от самой кислоты HNO 3ее соли — нитратыпроявляют сильные окислительные свойства только при сплавлении за счет выделяющегося кислорода. При нагревании нитраты разлагаются по-разному, в зависимости от положения металла в ряду напряжений:

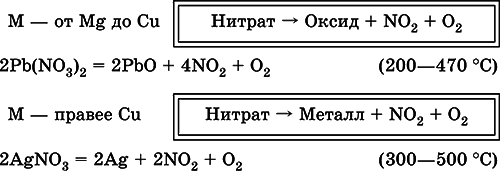
Применяется азотная кислота для производства минеральных удобрений, взрывчатых веществ, нитратов металлов, органических нитропроизводных, искусственных волокон и пластмасс, красителей, лекарственных препаратов.
Уравнения важнейших реакций:
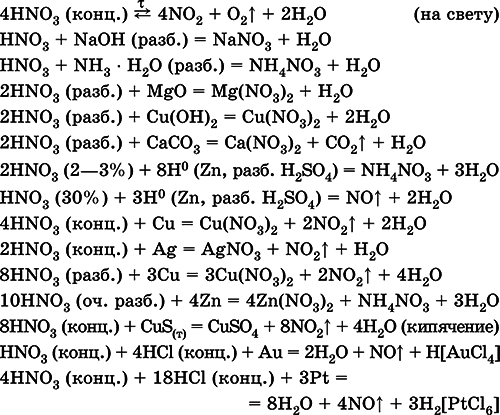
Получение: промышленныйсинтез состоит из следующих этапов:
N 2+ Н 2> NH 3> NO > NO 2> HNO 3> HNO 3,
а именно: производство аммиака (см.), каталитическое окисление аммиака (см.) до NO, перевод NO (см.) в NO 2, поглощение смеси NO 2и O 2водой (см.).
7.4.3. Нитриты. Нитраты
Нитрит калия KNO 2. Оксосоль. Белый, гигроскопичный. Плавится без разложения. Устойчив в сухом воздухе. Очень хорошо растворим в воде (образуется бесцветный раствор), гидролизуется по аниону. Типичный окислитель и восстановитель в кислотной среде, очень медленно реагирует в щелочной среде. Вступает в реакции ионного обмена. Качественные реакциина ион NO 2 -– обесцвечивание фиолетового раствора MnO 4и появление черного осадка при добавлении ионов I -. Применяется в производстве красителей, как аналитический реагент на аминокислоты и иодиды, компонент фотографических реактивов.
Уравнения важнейших реакций:
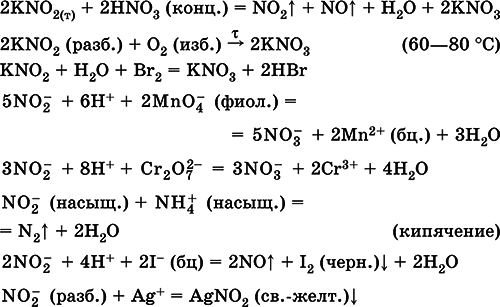
Получениев промышленности– восстановлением калийной селитры в процессах:
KNO 3+ Pb = KNO 2+ PbO (350–400 °C)
KNO 3(конц.) + Pb (губка) + Н 2O = KNO 2+ Pb(OH) 2v
2KNO 3+ СаО + SO 2= 2 KNO 2+ CaSO 4 (300 °C)
Нитрат калияKNO 3.Оксосоль. Техническое название калийная,или индийская, селитра.Белый, плавится без разложения, при дальнейшем нагревании разлагается. Устойчив на воздухе. Хорошо растворим в воде (с высоким эндо-эффектом, Q = -36 кДж), гидролиза нет. Сильный окислитель при сплавлении (за счет выделения атомарного кислорода). В растворе восстанавливается только атомарным водородом (в кислотной среде до KNO 2, в щелочной среде до NH 3).
Применяется в производстве стекла, как консервант пищевых продуктов, компонент пиротехнических смесей и минеральных удобрений.
Уравнения важнейших реакций:
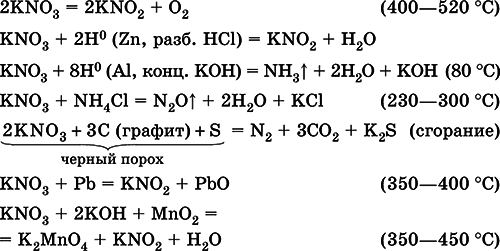
Получение: в промышленности
4KOH (гор.) + 4NO 2+ O 2= 4 KNO 3+ 2Н 2O
и в лаборатории:
КCl + AgNO 3= KNO 3+ AgClv
7.4.4. Фосфор
Фосфор– элемент 3-го периода и VA-группы Периодической системы, порядковый номер 15. Электронная формула атома [ 10Ne]3s 23p 3, устойчивая степень окисления в соединениях +V.
Шкала степеней окисления фосфора:
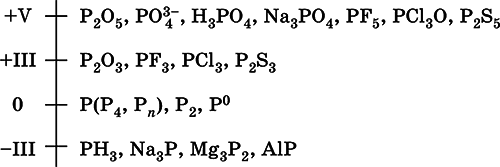
Электроотрицательность фосфора (2,32) значительно ниже, чем у типичных неметаллов, и немного выше, чем у водорода. Образует различные кислородсодержащие кислоты, соли и бинарные соединения, проявляет неметаллические (кислотные) свойства. Большинство фосфатов нерастворимы в воде.
В природе – тринадцатыйпо химической распространенности элемент (шестой среди неметаллов), встречается только в химически связанном виде. Жизненно важный элемент.
Недостаток фосфора в почве восполняется введением фосфорных удобрений – главным образом суперфосфатов.
Красный и белый фосфорР.Известно несколько аллотропных форм фосфора в свободном виде, главные – это белый фосфорР 4и красный фосфорР n. В уравнениях реакций аллотропные формы представляют как Р (красн.) и Р (бел.).
Красный фосфор состоит из полимерных молекул Р nразной длины. Аморфный, при комнатной температуре медленно переходит в белый фосфор. При нагревании до 416 °C возгоняется (при охлаждении пара конденсируется белый фосфор). Нерастворим в органических растворителях. Химическая активность ниже, чем у белого фосфора. На воздухе загорается только при нагревании.
Применяется как реагент (более безопасный, чем белый фосфор) в неорганическом синтезе, наполнитель ламп накаливания, компонент намазки коробка при изготовлении спичек. Не ядовит.
Белый фосфор состоит из молекул Р 4. Мягкий как воск (режется ножом). Плавится и кипит без разложения (t пл44,14 °C, t кип287,3 °C, ? 1,82 г/см 3). Окисляется на воздухе (зеленое свечение в темноте), при большой массе возможно самовоспламенение. В особых условиях переводится в красный фосфор. Хорошо растворим в бензоле, эфирах, сероуглероде. Не реагирует с водой, хранится под слоем воды. Чрезвычайно химически активен. Проявляет окислительно-восстановительные свойства. Восстанавливает благородные металлы из растворов их солей.
Применяется в производстве Н 3РO 4и красного фосфора, как реагент в органических синтезах, раскислитель сплавов, зажигательное средство. Горящий фосфор следует гасить песком (но не водой!). Чрезвычайно ядовит.
Уравнения важнейших реакций:
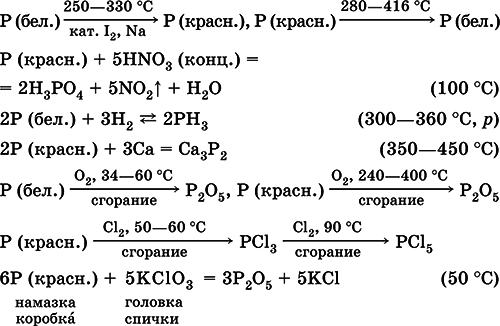
Получениев промышленности– восстановление фосфорита раскаленным коксом (песок добавляют для связывания кальция):
Са 3(РO 4) 2+ 5С + 3SiO 2= 3CaSiO 3+ 2 Р+ 5СО (1000 °C)
Пар фосфора охлаждают и получают твердый белый фосфор.
Красный фосфор готовят из белого фосфора (см. выше), в зависимости от условий степень полимеризации n (Р n) может быть различной.
ФосфинРН 3.Бинарное соединение, степень окисления фосфора равна – III. Бесцветный газ с неприятным запахом. Молекула имеет строение незавершенного тетраэдра [: Р(Н) 3] (sр 3-гибридизация). Мало растворим в воде, не реагирует с ней (в отличие от NH 3). Сильный восстановитель, сгорает на воздухе, окисляется в HNO 3(конц.). Присоединяет HI. Применяется для синтеза фосфорорганических соединений. Сильно ядовит.
Уравнения важнейших реакций: