М + H 2SO 4(pasб.) = MSO 4+ Н 2^ (М = Be, Mg, Cr, Mn, Zn, Fe, Ni)
2M + 3H 2SO 4(paзб.) = M 2(SO 4) 3+ 3H 2^ (M = Al, Ga)
3M + 2Н 3РO 4(разб.) = M 3(PO 4) 2v + 3H 2^ (M = Mg, Fe, Zn)
В отличие от бескислородных кислот кислотные гидроксиды называют кислородсодержащими кислотами или оксокислотами.
Амфотерные гидроксидыобразованы элементами с амфотерными свойствами. Типичные амфотерные гидроксиды:
Be(OH) 2Sn(OH) 2Al(OH) 3AlO(OH)
Zn(OH) 2Pb(OH) 2 Cr(OH) 3CrO(OH)
He образуются из амфотерных оксидов и воды, но подвергаются реальной дегидратации и образуют амфотерные оксиды:
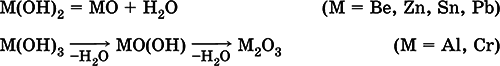
Исключение: для железа(III) известен только метагидроксид FeO(OH), «гидроксид железа(III) Fe(OH) 3» не существует (не получен).
Амфотерные гидроксиды проявляют свойства основных и кислотных гидроксидов; образуют два вида солей, в которых амфотерный элемент входит в состав либо катионов солей, либо их анионов.
Для элементов, имеющих несколько степеней окисления, действует правило: чем выше степень окисления, тем более выражены кислотные свойства гидроксидов (и/или соответствующих оксидов).
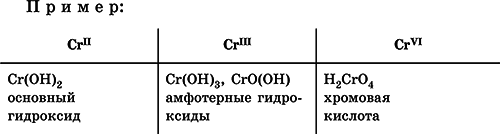
Соли– соединения, состоящие из катионовосновных или амфотерных (в роли основных) гидроксидов и анионов(остатков) кислотных или амфотерных (в роли кислотных) гидроксидов. В отличие от бескислородных солей, соли, рассматриваемые здесь, называются кислородсодержащими солямиили оксосолями.Делятся по составу катионов и анионов:
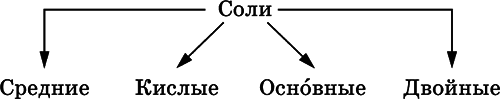
Средние солисодержат средние кислотные остатки СО 3 2-, NO 3 -, РО 4 3-, SO 4 2-и др.; например: К 2СO 3, Mg(NO 3) 2, Cr 2(SO 4) 3, Zn 3(PO 4) 2.
Если средние соли получают по реакциям с участием гидроксидов, то реагенты берут в эквивалентных количествах. Например, соль К 2СO 3можно получить, если взять реагенты в соотношениях:
2КОН и 1Н 2СO 3, 1К 2O и 1Н 2СO 3, 2КОН и 1СO 2.
Реакции образования средних солей:
1)
1а) основный гидроксид + кислотный гидроксид >…
2NaOH + H 2SO 4= Na 2SO 4+ 2Н 2O
Cu(OH) 2+ 2HNO 3= Cu(NO 3) 2+ 2H 2O
1б) амфотерный гидроксид + кислотный гидроксид >…
2Al(ОН) 3+ 3H 2SO 4= Al 2(SO 4) 3+ 6Н 2O
Zn(OH) 2+ 2HNO 3= Zn(NO 3) 2+ 2Н 2O
1в) основный гидроксид + амфотерный гидроксид >…
NaOH + Al(ОН) 3= NaAlO 2+ 2Н 2O (в расплаве)
2NaOH + Zn(OH) 2= Na 2ZnO 2+ 2Н 2O (в расплаве)
2)
2а) основный оксид + кислотный гидроксид >…
Na 2O + H 2SO 4= Na 2SO 4+ Н 2O
CuO + 2HNO 3= Cu(NO 3) 2+ H 2O
2б) амфотерный оксид + кислотный гидроксид >…
Al 2O 3+ 3H 2SO 4= Al 2(SO 4) 3+ 3H 2O
ZnO + 2HNO 3= Zn(NO 3) 2+ H 2O
2в) основный оксид + амфотерный гидроксид >…
Na 2O + 2Al(ОН) 3= 2NaAlO 2+ ЗН 2O (в расплаве)
Na 2O + Zn(OH) 2= Na 2ZnO 2+ Н 2O (в расплаве)
3)
За) основный гидроксид + кислотный оксид >…
2NaOH + SO 3= Na 2SO 4+ Н 2O
Ва(ОН) 2+ СO 2= ВаСO 3+ Н 2O
3б) амфотерный гидроксид + кислотный оксид >…
2Al(ОН) 3+ 3SO 3= Al 2(SO 4) 3+ 3H 2O
Zn(OH) 2+ N 2O 5= Zn(NO 3) 2+ H 2O
Зв) основный гидроксид + амфотерный оксид >…
2NaOH + Al 2O 3= 2NaAlO 2+ Н 2O (в расплаве)
2NaOH + ZnO = Na 2ZnO 2+ Н 2O (в расплаве)
4)
4а) основный оксид + кислотный оксид >…
Na 2O + SO 3= Na 2SO 4, BaO + СO 2= ВаСO 3
4б) амфотерный оксид + кислотный оксид >…
Al 2O 3+ 3SO 3= Al 2(SO 4) 3, ZnO + N 2O 5= Zn(NO 3) 2
4в) основный оксид + амфотерный оксид >…
Na 2O + Al 2O 3= 2NaAlO 2, Na 2O + ZnO = Na 2ZnO 2
Реакции 1в, если они протекают в растворе, сопровождаются образованием других продуктов — комплексных солей:
NaOH (конц.) + Al(OН) 3= Na[Al(OH) 4]
КОН (конц.) + Cr(OH) 3= К 3[Cr(ОН) 6]
2NaOH (конц.) + M(OH) 2= Na 2[M(OH) 4] (М = Be, Zn)
КОН (конц.) + M(OH) 2= K[M(OH) 3] (М = Sn, Pb)
Все средние соли в растворе – сильные электролиты (диссоциируют нацело).
Кислые солисодержат кислые кислотные остатки (с водородом) HCO 3 -, Н 2РO 4 2-, HPO 4 2-и др., образуются при действии на основные и амфотерные гидроксиды или средние соли избытка кислотных гидроксидов, содержащих не менее двух атомов водорода в молекуле; аналогично действуют соответствующие кислотные оксиды:
NaOH + H 2SO 4(конц.) = NaHSO 4+ H 2O
Ва(ОН) 2+ 2Н 3РO 4(конц.) = Ва(Н 2РO 4) 2+ 2Н 2O
Zn(OH) 2+ Н 3РO 4(конц.) = ZnHPO 4v + 2Н 2O
PbSO 4+ H 2SO 4(конц.) = Pb(HSO 4) 2
K 2HPO 4+ Н 3РO 4(конц.) = 2КН 2РO 4
Са(ОН) 2+ 2ЕO 2= Са(НЕO 3) 2(Е = С, S)
Na 2EO 3+ ЕO 2+ H 2O = 2NaHEO 3(Е = С, S)
При добавлении гидроксида соответствующего металла или амфигена кислые соли переводятся в средние:
NaHSO 4+ NaOH = Na 2SO 4+ Н 2O